 | |
| Nama | |
|---|---|
| Nama IUPAC
Renium(IV) oksida
| |
| Nama lain
Renium dioksida
| |
| Pengecam | |
Imej model 3D Jmol
|
|
| ECHA InfoCard | 100.031.659 |
| Nombor EC |
|
PubChem CID
|
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Sifat | |
| ReO2 | |
| Jisim molar | 218.206 g/mol |
| Rupa bentuk | Hablur ortorombus kelabu |
| Ketumpatan | 11.4 g/cm3[1] |
| Takat lebur | Terurai pada 1000 °C[2] |
| Tidak larut | |
| Keterlarutan dalam alkali | Tidak larut |
| +44.0·10−6 cm3/mol | |
| Struktur | |
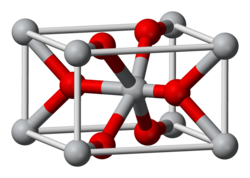
| Struktur kristal | Ortorombus, oP12 |
| Kumpulan ruang | Pbcn, No. 60 |
| Bahaya | |
| MSDS | Aldrich MSDS |
| NFPA 704 (berlian api) | |
| Sebatian berkaitan | |
Anion lain
|
Renium(VII) oksida Renium(III) oksida Renium(III) klorida |
Kation lain
|
Mangan(IV) oksida Teknetium(IV) oksida |
Kecuali jika dinyatakan sebaliknya, data diberikan untuk bahan-bahan dalam keadaan piawainya (pada 25 °C [77 °F], 100 kPa). | |
| | |
| Rujukan kotak info | |
Renium(IV) oksida atau renium dioksida ialah sebatian kimia renium dengan formula kimia ReO2. Sebatian ini berwarna kelabu kehitaman dan digunakan sebagai mangkin dalam persekitaran makmal.
Penghasilan
Renium(IV) oksida boleh dihasilkan melalui tindak balas antara renium(VII) oksida dan logam renium.[3]
Selain itu, renium(IV) oksida boleh dihasilkan melalui pemanasan ammonium perenat, NH4ReO4 dalam persekitaran udara nitrogen atau argon kering serta dalam vakum.[4]
Tindak balas
Dalam suhu yang tinggi, sebatian ini boleh terurai semula kepada renium(VII) oksida dan logam renium.
Renium(IV) oksida bertindak balas dengan natrium hidroksida lebur untuk menghasilkan natrium renat.[5]
Rujukan
- ^ Lide, David R. (1998). Handbook of Chemistry and Physics (ed. 87). CRC Press. m/s. 484. ISBN 0-8493-0594-2. Dicapai pada 2008-06-05.
- ^ Perry, Dale L.; Phillips, Sidney L. (1995). Handbook of Inorganic Compounds. San Diego: CRC Press. m/s. 328. ISBN 0-8493-8671-3. Dicapai pada 2008-06-05.
- ^ G. Glemser "Rhenium (IV) Oxide" Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 1480.
- ^ Brauer, Georg (1981). "3., umgearbeitete Auflage". Handbuch der Präparativen Anorganischen Chemie (dalam bahasa Jerman). III. Stuttgart: Ferdinand Enke. m/s. 1617. ISBN 3-432-87823-0.
- ^ G. Glemser "Sodium Rhenate (IV)" Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 1483.










![{\displaystyle {2\,\mathrm {Re} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{7}}{}+{}3\,\mathrm {Re} {}\mathrel {\longrightarrow } {}7\,\mathrm {ReO} {\vphantom {A}}_{\smash[{t}]{2}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7b6f053afb8bdaede7d4c6846201471b4c615ae0)
![{\displaystyle {\mathrm {NH} {\vphantom {A}}_{\smash[{t}]{4}}\mathrm {ReO} {\vphantom {A}}_{\smash[{t}]{4}}{}\mathrel {\longrightarrow } {}2\,\mathrm {ReO} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {N} {\vphantom {A}}_{\smash[{t}]{2}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/7ecbaf45f847e65bb3d2a4c7a24e74751196942d)
![{\displaystyle {7\,\mathrm {ReO} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}2\,\mathrm {Re} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} {\vphantom {A}}_{\smash[{t}]{7}}{}+{}3\,\mathrm {Re} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c74ec794494b5f4c6cf413279b11c6bfbe702385)
![{\displaystyle {2\,\mathrm {NaOH} {}+{}\mathrm {ReO} {\vphantom {A}}_{\smash[{t}]{2}}{}\mathrel {\longrightarrow } {}\mathrm {Na} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {ReO} {\vphantom {A}}_{\smash[{t}]{3}}{}+{}\mathrm {H} {\vphantom {A}}_{\smash[{t}]{2}}\mathrm {O} }}](https://wikimedia.org/api/rest_v1/media/math/render/svg/85f35c13efedbebc2de9d86123b7491384f9a640)